Классификация реактивов
Химические реактивы – это вещества, которые используются в химических лабораториях для анализа веществ, приготовления растворов, проведения реакции, изготовлении красителей, моющих средств.
Классифицировать химические реактивы можно по степени чистоты, областям использования, по свойствам реактивов:
-
В зависимости от содержания основного вещества и допустимых примесей химические реактивы имеют следующие марки чистоты:
- Технический (тех.)
- Чистый (ч.)
- Чистый для анализа (ч.д.а.)
- Химически чистый (х.ч.)
- Особо чистый (ос.ч.)
Технические реактивы – это реактивы, содержащие в себе около 5% примесей и только 95% основного вещества.
Чистые реактивы содержат в себе от 98% основного вещества.
Чистый для анализа реактив должен содержать в себе много больше 99% основного компонента и минимальное количество примесей.
Xимически чистые реактивы являются высшей степенью чистоты реактива с содержанием примесей 10⁻³-10⁻⁵%.
Особо чистые реактивы содержание примесей не превышает 10⁻⁵-10⁻¹⁰%.

-
По областям применения реактивы классифицируются на:
-
Общеупотребительные индикаторы
-
Красители для микроскопии
-
Краситель для хроматографии
-
-
По свойствам реактивы делятся на:
-
Гидроскопичные(влагочувствительные)
-
Светочувствительные
-
Пожароопасные
-
Ядовитые
-

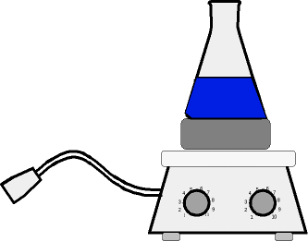
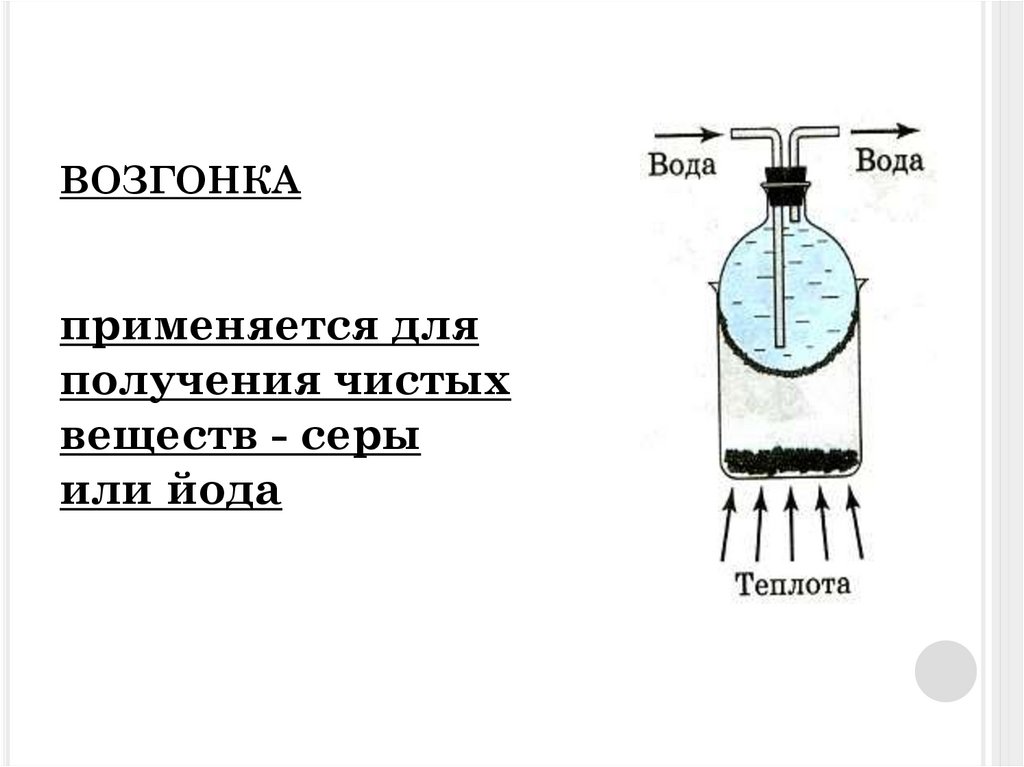
Методы очистки. Возгонка
Возгонка - это переход вещества из твердого в газообразное состояние, минуя стадию жидкости. Точно так же пары вещества могут конденсироваться, минуя жидкое состояние, образуя непосредственно кристаллы.
Возгонка – способ очистки веществ в тех случаях, когда примеси обладают иной летучестью, чем само вещество, и заменяют длительную и трудоёмкую кристаллизацию. Очищенное таким образом вещество свободно от примесей, поэтому возгонку часто используют в качестве конечной операции при получении образцов для анализа. Этот метод удобен для очистки веществ, образующих сольваты и гидраты.

Хранение реактивов
Все химические вещества, находящиеся в лаборатории должны быть снабжены этикетками с названием соединения и его формулами.

Запрещается использовать и хранить вещества без этикеток. если невозможно установить формулу вещества, то такой реактив должен быть уничтожен.
Необходимые обозначения на этикетке:
-
название вещества
-
масса реактива
-
классификация
-
номер партии
-
дата изготовления
Все реактивы должны быть упакованы в соответствующую потребительскую тару, герметически упакованную и снабженную этикеткой.
Для реактивов каждой классификации этикетка на таре должна быть определенного цвета или на ней должна быть цветная полоса:
| Классификация реактивов | Цвет этикетки |
|---|---|
| Чистый | Зеленый |
| Чистый для анализа | Синий |
| Химически чистый | Красный |
| Особо чистый | Желтый |
-
Химические реактивы должны храниться в специально оборудованных, хорошо вентилируемых, сухих помещениях (складах) согласно разработанной в лаборатории схеме размещения реактивов.
-
При размещении реактивов следует соблюдать порядок совместного хранения пожаро- и взрывоопасных веществ. Не разрешается совместное хранение реактивов, способных реагировать друг с другом с выделением тепла или горючих газов. Запрещается также совместно хранить вещества, которые в случае возникновения пожара нельзя тушить одним огнетушащим средством.
-
Запрещается расфасовывать сыпучие вещества на складе.

Методы очистки. Дистилляция
Дистилляция — способ разделения или очистки веществ, основанный на различные температуры кипения.
При дистилляции жидкость путем нагревания переводят в парообразное состояние, затем снова конденсируют, т.е. превращают в жидкость.
Установка для для простой дистилляции состоит из перегонной колбы 1, снабженной термометром 2, водяного холодильника 3, алонжа 4 и приемной колбы 5.


Правила работы с реактивами

Правила пользования реактивами:
- Главное требование к реактивам – это их чистота
- Нельзя ссыпать и сливать реактив из посуды, в которой проводится реакция, обратно в посуду для хранения
- Нельзя путать пробки от посуды с разными реактивами
Правила работы с кислотами и щелочами:
- Все концентрированные растворы должны храниться в специальных бутылях с притертыми пробками. Щелочи хранят в широкогорлых банках из темного стекла
- Посуда, в которой хранятся кислоты и щелочи, должна иметь четкие написи
- Работать с концетрированными кислотами и щелочами разрешается только в вытяжном шкафу с включенной принудительной вентиляцией
- Бутыли с кислотами и щелочами необходимо переносить вдвоем в специальных корзинах или ящиках
- При приготовлении растворов кислот, кислоту приливают к воде, а не наоборот
Чистые вещества и смеси. Методы разделения и очистки веществ.
Чистое вещество содержит частицы только одного вида. Примерами могут служить серебро (содержит только атомы серебра), серная кислота и оксид углерода (IV) (содержат только молекулы соответствующих веществ). Все чистые вещества имеют постоянные физические свойства, например, температуру плавления (Тпл) и температуру кипения (Ткип).
Вещество не является чистым, если содержит какое-либо количество одного или нескольких других веществ – примесей. Загрязнения понижают температуру замерзания и повышают температуру кипения чистой жидкости. Например, если в воду добавить соль, температура замерзания раствора понизится.
Смеси состоят из двух или более веществ. Почва, морская вода, воздух – все это примеры различных смесей. Многие смеси могут быть разделены на составные части – компоненты – на основании различия их физических свойств.
Традиционными методами, которые используются в лабораторной практике с целью разделения смесей на отдельные компоненты, являются:
- фильтрование,
- отстаивание с последующей декантацией,
- разделение с помощью делительной воронки,
- центрифугирование,
- выпаривание,
- кристаллизация,
- перегонка (в том числе фракционная перегонка),
- хроматография,
- возгонка и другие.


Фильтрование
Фильтрование - это разделение неоднородных систем с помощью пористых перегородок - фильтров.
В качестве фильтров обычно используют фильтровальную бумагу, которая может быть различной пористости.
Фильтрами могут служить также различные ткани, пористое стекло, асбест, обычная и стеклянная вата и др.
Сборка установки для фильтрования
При фильтровании воронку укрепляют на кольце штатива. Кончик воронки должен касаться стенки сосуда для фильтрата.
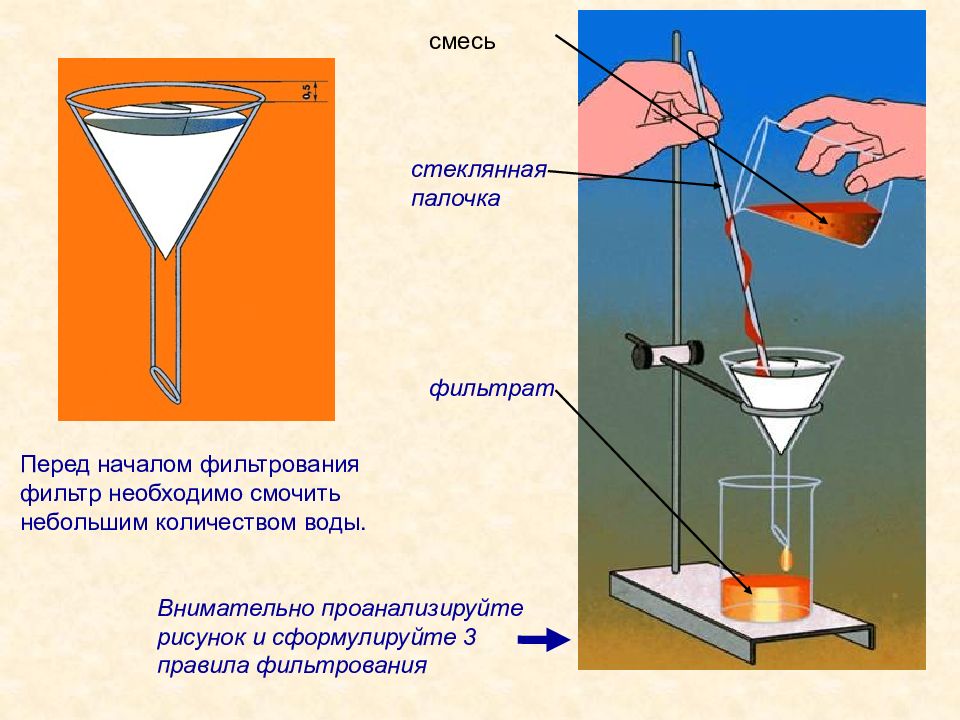
Жидкость выливают по стеклянной палочке, прижимая ее к стенке воронки. Для ускорения фильтрования на фильтре следует поддерживать высокий уровень жидкости, подливая ее небольшими порциями. Затем осадок промывают несколько раз, используя по возможности малые количества растворителя, так как при промывании, хотя и незначительная часть осадка переходит в раствор. Новую порцию жидкости на фильтр наливают, только после того, как предыдущая будет полностью отфильтрована.
Методы очистки. Перекристаллизация.
Метод основан на различной растворимости вещества и сопутствующих ему примесей в данном растворителе при различных температурах.
Стадии перекристаллизациятвердого вещества состоит из следующих стадий:
- приготовление горячего насыщенного раствора при нагревании;
- адсорбция некоторых примесей на сорбенте;
- горячее фильтрование раствора;
- кристаллизация при полном охлаждении;
- фильтрование при пониженном давлении;
- сушка.
В качестве растворителей могут применяться этиловый спирт, ацетон, бензол, диоксан, уксусная кислота, вода и др. Если данные о растворимости очищаемого вещества отсутствуют, то растворитель подбирают опытным путем по принципу «подобное к подобному». Хорошо подобранный растворитель при температуре, близкой к точке кипения, должен растворять, по крайней мере, в пять раз больше вещества, чем при комнатной температуре. Иногда, если очищаемое вещество хорошо растворяется в растворителе при нагревании, но плохо из него осаждается при охлаждении, кристаллизацию проводят из смеси различных растворителей, умело подобрав их соотношение.
В общем случае необходимо учитывать следующие требования к растворителям:
- растворитель должен быть химически инертен по отношению к основному веществу и к примесям;
- растворитель должен быть избирателен, т.е. растворять основное вещество в 2-4 раза лучше, чем примеси (или наоборот);
- растворитель должен хорошо растворять вещество, т.е. примерно 1 г вещества в 100 г растворителя;
- растворитель должен растворять вещество при нагревании в 2-4 раза лучше, чем при комнатной температуре;
- растворитель должен быть наиболее безопасным, т.е. наименее взрыво-пожароопасным, токсичным.